¿Sabía usted que la Silimarina: calma el “síndrome de tormenta de citoquinas” y disminuirá la mortalidad?
Escribe: Dr. Manuel Albetis Apolaya
Docente Universidad Nacional San Luis Gonzaga de Ica - Perú
Asesor técnico / Veterinario FARVET
Introducción
Ya se tiene bien claro que los predictores de un desenlace fatal en los casos de COVID-19 incluyeron la edad, la presencia de enfermedades subyacentes, la presencia de infección secundaria y los indicadores inflamatorios elevados en la sangre. Los resultados obtenidos por estudios también sugieren que la mortalidad de COVID-19 podría deberse a un «síndrome de tormenta de citoquinas» activado por virus o miocarditis fulminante. (1).
Como todo proceso viral, el tratamiento que se usa para el COVID-19 es de apoyo, y la principal causa de muerte es la insuficiencia respiratoria aguda.
Síndrome de tormenta de citoquinas
Existe según Karakike et,al., la linfocitosis hemofagocitica (HLH) que se caracteriza por citocina fulminante tormenta que conduce a la disfunción de múltiples órganos y alta mortalidad. HLH se clasifica en familiar (fHLH) y secundaria (sHLH). El primero es raro y se debe a mutaciones de genes que codifican para perforina o gránulos excretores de células asesinas naturales (NK) de linfocitos CD8 pero las más importante en este caso la sHLH que se conoce también como síndrome de activación de macrófagos (MAS). Este síndrome se caracteriza porque presenta fiebre, hepatoesplenomegalia, disfunción hepatobiliar, cuagulopatia, citopenia de 2.3 linajes celulares, aumento de triglicéridos y hemofagocitosis en la médula osea. sHLH/MAS complica neoplasias hematológicas, trastornos autoinmunes y lo principal en este caso infecciones de origen viral. De lo que se sabe hasta ahora es que se asocia con una mayor activación de macrófagos y células NK, citosina tormenta de IL-6, IL-18, ferritina e interferón gamma. El CD163 soluble aumenta mucho a partir de los macrófagos. (2).
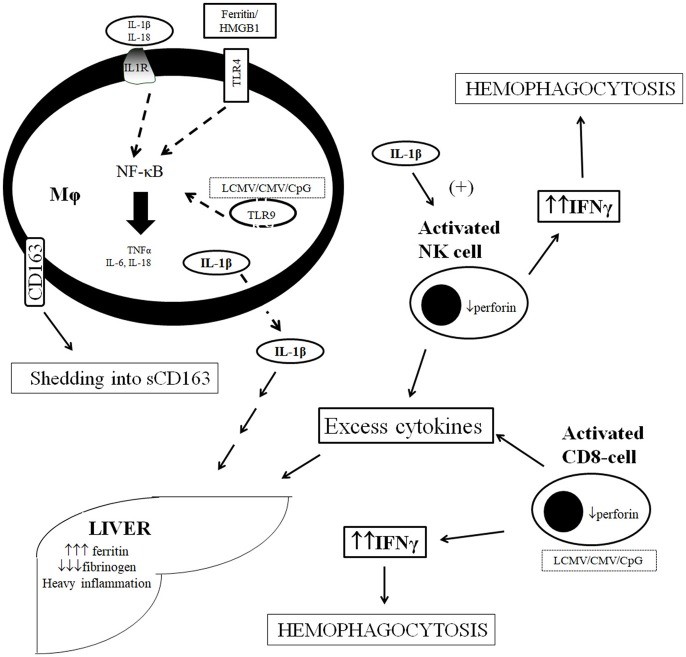
Patogénesis hipotética del COVID-19
Lin et, al., en marzo del 2020 en base a las literaturas y observaciones clínicas en paciente con COVID-19, propone una hipótesis razonable sobre la patogénesis de la infección por SARS-CoV-2 en humanos. Ellos indican que puede pasar a través de las membranas mucosas, (nasal y laríngea), luego a los pulmones a través del tracto respiratorio. Los primeros síntomas más comunes de infección son fiebre y tos (3), pasa el virus a la sangre causando una viremia y de ahí pasa a atacar a los órganos que expresan la proteína receptora (ACE2), dentro de ellas los pulmones, el corazón, el riñón, el tracto gastrointestinal, tal como lo manifiesta Letko en el 2020 (4). La condición del paciente se agrava alrededor de 7 a 14 días. En pacientes de tipo grave, los linfocitos se reducen significativamente (3), pero lo que más importa en este artículo es que factores inflamatorios asociados con enfermedades que contienen, principalmente IL-6 aumentan drásticamente (5), esto es lo que contribuye al agravamiento de la enfermedad alrededor de 7 a 14 días después del inicio. Wang indica algo muy importante, los no sobrevivientes tenían niveles más alto de neutrófilos, D-D-imer, notrogeno urico en sangre y creatinina que los que sobrevivieron (6).
La fase clínica de la enfermedad se divide en tres: la fase de viremia, la fase aguda (fase de neumonía) y la fase de recuperación. Si el paciente es mayor, o está en un estado de inmunodeficiencia, combinado con otras enfermedades básicas como la hipertensión y la diabetes, el sistema inmunitario no va a poder controlar al virus en la fase de neumonía, y este se convierte en un tipo crítico. En esta situación las células T, las células B se reducen más, y aquí ocurre algo muy importante. Las citosinas inflamatorias y el Dímero D continúan en ascenso. Por lo que Ling indica claramente que para mejorar la función inmune de los pacientes es inhibir la formación de tormentas de factores inflamatorios. El propone el uso de la terapia anticuagulantes IVIg y de Heparina de bajo peso molecular (HBPM) y que se administre antes de estos sucesos, más que todo para interrumpir la tormenta de factores inflamatorios en una etapa temprana, mejorar la función inmune en pacientes con COVID-19-, concluyendo que el tratamiento actual de pacientes con COVID-19 con tipo grave y tipo crítico es la clave para controlar el creciente número de muertes, que esta mediada por la tendencia de las células T, células B, citoquinas inflamatorias, Dímero D después de la terapia. Por lo que recomienda más investigación relacionada con el sistema inmunitario y comprender la patogénesis, y guiar el tratamiento de la enfermedad y mejorar el pronóstico.

Ventilación mecánica
Otro factor recientemente se ha demostrado como capaz de inducir a una respuesta inflamatoria, es el uso de ventilación mecánica. Raniere y col en 1999, ellos optaron por una estrategia protectora, la cual demostró una menor activación de la respuesta inflamatoria que la ventilación “convencional”. Este efecto indica que podría estar mediado por una menor sobre distensión pulmonar así como por una reducción de fenómenos de reclutamiento alveolar-derreclutamiento alveola (7).
Citoquinas
La definición de citoquinas puede basarse en términos generales en su función como señales intercelulares (8). Pueden ser proteínas secretadas o asociadas a la superficie celular que interactúan con receptores específicos de la superficie celular que resultan en la movilización y / o modulación de las células diana. Es un inmunomodulador, ya que las citocinas pueden tener efectos estimulantes o supresores en las células huésped. Las citocinas usualmente, pero no siempre, actúan localmente en un rango corto en los tejidos, ya sea en forma paracrina o incluso en forma autocrina. Cuando las citocinas se producen en abundancia debido a infecciones abrumadoras, reacciones autoinmunes o lesiones, pueden extenderse al suero y tener efectos globales, como fiebre y cambios de comportamiento, y pueden tener efectos nocivos, como «tormenta de citoquinas, liberación de citocinas». o síndrome de activación de macrófagos ” (9). Este síndrome potencialmente letal se puede tratar con reactivos antiinflamatorios como los esteroides, anti-interleucina (IL) -6 o anakinra, un antagonista de la IL-1 (10). Incluso existen evidencia considerable de que los virus producen imitaciones de citoquinas para su propio beneficio (11).
Una citocina es una señal que nunca ocurre sola, es parte de un entorno complejo. Dependiendo de la mezcla, podemos repeler a un invasor o autodestruirnos.
CONSECUENCIA DE LOS MEDIADORES INFLAMATORIOS
- Células epiteliales y endoteliales de los pulmones sufre apoptosis.
- Interferones tipo I y II favorecen este efecto.
- Resultado fuga vascular y edema alveolar – hipoxia
- Infiltración de monocitos/macrófagos inflamatorios (IMM)
- Mayor liberación de mediadores inflamatorios y daño
- Respuesta de célula T subóptima.
- Las células T contribuyen al aclaramiento de la infección viral y limitación del daño al huésped
- La apoptosis de linfocitos T (mediados por TNF y INF-I) favorece una respuesta inflamatoria mal regulada
Hannappanavar R y Perlman S 2017 (12)
Lo que realmente se sabe de las citoquinas es que la gravedad se asocia con el incremento de IL – 12, IL-7, MCP-I, IL.10. (13). Tal como se observa en la figura donde se observa claramente que pacientes que entraron a el estado crítico los niveles de estas citoquinas se incrementaron, comparados con el control y los que no entraron al estado crítico (13).

Huang C, Lancet 2020
En el siguiente grafico se aprecia en primera instancia que cuando hay una respuesta temprana de IFN-I frente al virus, se reduce los títulos del virus. Hay una regulación de la inflamación. Manifestando una enfermedad clínica leve.

Cuando hay una señalización atrasada de IFN-I, presenta una disgularidad de la respuesta de IMM. Inmunopatología pulmonar y se presenta una neumonía letal: mientras que cuando no hay señalización de IFN-I frente al virus, se ve reducido la respuesta IMM, no manifiesta inmunopatología pulmonar y la enfermedad clínica es reducida. (14)
Con todo la manifestado esta bien claro la acción de las citoquinas, frente a la respuesta del virus el «síndrome de tormenta de citoquinas».
El “síndrome de tormenta de citoquinas” y los cambios a nivel de la expresión génica de las células.
Las citoquinas actúan a nivel celular de la siguiente manera
- Inician una cascada de transducción intracelular
- Señal que altera el patrón de expresión génica de modo que esas células diana producen una determinada respuesta biológica
- Las respuestas celulares a las citoquinas, frecuentemente, consisten en cambios en la expresión génica, con expresión de nuevas funciones o incluso proliferación celular
Al alterar la expresión genética de las células diana, (células alveolares), dejan de sintetizar proteínas para su regeneración y bien se acumulan de grasa y en este caso se fibrosa el pulmón. Por la acción lipogenica o fibrogenica de los órganos diana (14).
Cambios génicos por acción de las citoquinas activadas por virus y otros

Fuente: León et al, 2006.
Flavonoides
Los altos niveles de citocinas, como la interleucina (IL) -1β, el factor de necrosis tumoral (TNF) -α y la IL-6, están asociados con enfermedades crónicas como la artritis reumatoide, el asma, la aterosclerosis, la enfermedad de Alzheimer, el cáncer y el síndrome de activación de macrófagos (MAS) en este caso por acción del COVIOD-19; por lo tanto, la inhibición de citoquinas podría ser un objetivo importante para el tratamiento de estas enfermedades. Se ha mencionado que los flavonoides, a saber, quercetina, apigenina y luteolina, reducen la expresión y secreción de citoquinas. A este respecto, los flavonoides pueden tener potencial terapéutico en el tratamiento de enfermedades relacionadas con la inflamación como moduladores de citocinas. (16)
Los flavonoides son un grupo diverso de fitonutrientes (químicos vegetales) que se encuentran en muchas frutas, verduras y especias, según lo define el sitio especializado LiveScience en el 2015. (16)
Al igual que otros fitonutrientes, los flavonoides son poderosos antioxidantes, con características antiinflamatorias que está relacionado con el sistema inmunológico (17)
Silimarina/Silibina
El cardo mariano (Silybum marianum) es una planta medicinal que se ha utilizado durante miles de años como remedio para una variedad de dolencias. El componente principal del extracto de fruta de S. marianum (silimarina) es un flavonolignano llamado silibina, que no solo es el principal elemento de silimarina, sino que también es el ingrediente más activo de este extracto La estructura de Silibina consiste en dos unidades principales. El primero se basa en una taxifolina, el segundo en una unidad fenilpropanoide, que en este caso es alcohol conyferil. Estas dos unidades están unidas en una estructura por un anillo oxerano (19).
Estructura química del silibina

Cardo mariano

Silibina y su acción contra las lesiones del pulmón, producida por inflamación a causas de citoquinas
La silibina es uno de los principales flavonoides producidos por el cardo mariano, que se ha utilizado en el tratamiento de enfermedades hepáticas. Zhang et al 2017, en el 2017 realizo un estudio para examinar los efectos protectores y los posibles mecanismos de acción de la silibina en la lesión pulmonar e inflamación inducida por lipopolisacárido (LPS). El pretratamiento de ratones con silibina inhibió significativamente el reclutamiento de células inflamatorias de las vías respiratorias inducidas por LPS, incluidos macrófagos, células T y neutrófilos. La producción de citocinas, como la interleucina-1β (IL-1β) y el factor de necrosis tumoral-α (TNF-α) en el líquido broncoalveolar y el suero también disminuyó después del tratamiento con silibina. Los niveles elevados de ARNm de citocinas inducidos por LPS en el tejido pulmonar fueron suprimidos por la silibina y también se mejoraron las alteraciones histológicas pulmonares. Además, los experimentos con células indicaron que la silibina disminuyó significativamente los niveles de ARNm y la secreción de IL-1β y TNF-α en las células THP-1. Además, los mecanismos responsables de estos efectos se atribuyeron al efecto inhibidor de la silibina sobre la señalización del factor nuclear κB (NF-κB) y el dominio de pirina de la familia NLR que contiene 3 (NLRP3) activación del inflamasoma. Los datos de nuestro estudio respaldan la utilidad de la silibina como un medicamento potencial para el tratamiento de la inflamación aguda asociada a la lesión pulmonar y los cambios patológicos. La silibina ejerce efectos protectores contra la lesión pulmonar mediante la regulación de la señalización de NF-κB y la activación del inflamasoma NLRP3 (20).

El tratamiento con silibina previene la inflamación pulmonar inducida por lipopolisacárido (LPS) en ratones. (A) Los niveles de citocinas en el sobrenadante BALF y el suero de cada grupo de ratones se detectaron mediante un ensayo inmunoabsorbente ligado a enzimas (ELISA). Los valores se mostraron como las medias ± DE de 8 ratones. (B) Se extrajo ARN del tejido pulmonar de los ratones. (C) La expresión de ARNm de interleucina (IL) -6, factor de necrosis tumoral-α (TNF-α), IL-1β e IL-17 fue examinada por RT-qPCR. Los valores se mostraron como las medias ± DE de 8 ratones. * P <0.05 y ** P <0.01 vs. ratones expuestos a LPS solo. Zhang et al 2017.
Tian L, et al, 2017, realizaron un estudio para explorar los efectos terapéuticos y los posibles mecanismos de la silibinina en las respuestas inflamatorias estimuladas por lipopolisacárido (LPS) en la lesión pulmonar aguda (ALI). Los ratones BALB / c machos se acondicionaron con silibinina 1 h después de la instilación intranasal de LPS. Después de 12 h, se detectó el nivel de mieloperoxidasa (MPO) en los tejidos pulmonares, la relación húmeda / seco (W / D), las citocinas inflamatorias en el líquido de lavado broncoalveolar (BALF) y el examen histopatológico del pulmón. Sus resultados mostraron que la silibinina inhibió los cambios histopatológicos inducidos por LPS y la actividad MPO, así como la relación húmeda / seco (W / D) en los tejidos pulmonares. Además, la silibinina inhibió significativamente la producción de citocinas inflamatorias inducidas por LPS en el BALF. Además, la silibinina suprimió la activación de NF-κB inducida por LPS y la expresión de inflamasoma NLRP3. Estos resultados indican que la silibinina ejerce su efecto antiinflamatorio al inhibir las vías de señalización de NF-κB y NLRP3 (21).
Conclusiones
- La mortalidad de COVID-19 podría deberse a un “Síndrome de tormenta de citoquinas” o síndrome de activación de macrófagos a causa del virus.
- Para mejorar la función inmune de los pacientes hay que inhibir la formación de tormentas de factores inflamatorios.
- Por lo que es necesario usar terapias, que se administren antes de los sucesos, con la finalidad de interrumpir la tormenta de factores inflamatorios antes de estos sucesos dañinos y mejorar la función inmune en pacientes con COVID-19.
- ESTO SERIA LA CLAVE PARA CONTROLAR EL CRECIENTE NÚMERO DE MUERTE.
- Lo que realmente se sabe de las citoquinas, es que la gravedad se asocia con el incremento de IL-12, IL-7. MCP-I. IL-10 y los individuos que mueren estos se encuentran incrementados, comparados con los que no entraron en estado crítico.
- También se sabe con seguridad que cuando hay baja señal de IFN-1 frente al virus no se manifiesta inmunopatología pulmonar y la enfermedad clínica es reducida.
- El “síndrome de tormenta de citoquinas” produce cambios a nivel de expresión génica, modificancion el fenotipo celular y se incentiva a la lipogénesis y fibrogenesis, agudizando la degeneración pulmonar y no permitiendo su regeneración.
- Los flavonoides pueden tener un potencial terapéutico en el tratamiento de enfermedades relacionadas con inflamación con moduladores de citosinas.
- La silibina, es un flavolignano, ingrediente activo de la silimarina (Cardo mariano).
- Se ha demostrado en trabajos recientes, su acción contra lesiones del pulmón, producidas por inflamación de citoquinas y se encontró que inhibió significativamente el reclutamiento de células inflamatorias de las vías respiratorias; también inhibió la producción de citocinas, en el líquido broncoalveolar.
- Disminuyó significativamente los niveles de ARNm y la secreción de IL-1β y TNF-α en las células THP-1.
- Inhibe la señalización del factor nuclear κB (NF-κB) y el dominio de pirina de la familia NLR que contiene 3 (NLRP3) activación del inflamasoma
- Todo esto demuestra la utilidad de la silibina como un medicamento potencial para el tratamiento de la inflamación aguda asociada a la lesión pulmonar y los cambios patológicos.
- Por todo esto la silibina debe incluirse como protocolo para medicar en forma temprana y así reducir la muerte por COVID-19 en los pacientes más vulnerables.
Bibliografía
| 1. | Ruan Q, Kun Yang , Wenxia Wang , Lingyu Jiang , Jianxin Song. Clinical predictors of mortality due to COVID-19 based on an analysis of data of 150 patients from Wuhan, China. Intensive Care Med. 2020 Mar. |
| 2. | Karakike E, Giamarellos-Bourboulis E. Macrophage activation-like syndrome. Front Immuno. 2019; 10: p. 55. |
| 3. | Guan W, Ni Z Y , Hu Y, et al.. Clinical characteristics of 2019 novel coronavirus infection in China. N Engl J Med. 2020 Marzo; undefined: undefined. doi: 10.1056/NEJMoa2002032. |
| 4. | Letko M MA,MV. valoración funcional de la entrada en la célula y la utilización de receptor para el SARS-CoV-2 y otros betacoronaviruses linaje B. Nat Microbiol. 2020. |
| 5. | Wan S X YQJ,FSB,ea. Características de los subconjuntos de linfocitos y las citocinas en sangre periférica de 123 pacientes hospitalizados con neumonía por coronavirus novedosa (PCN) de 2019. medRxiv. 2020. |
| 6. | Wang D HB,Cyc. Características clínicas de 138 pacientes hospitalizados con neumonía infectada con coronavirus novela 2019 en Wuhan, hina. jama. 2020. |
| 7. | Ranieri V, Tortorella C, De Tulio R , Dayer J, Brianza A, et al. Effect of Mechanical Ventilation on inflammatory mediators in patients with Respiratory Distress Syndrome. A randomized controlled trial. JAMA. 1999; 282: p. 54-61. |
| 8. | Oppenheim JJ GI. From lymphodrek to interleukin 1 (IL-1). Immunol Today. 1993; 14(232-234). |
| 9. | Grom AA HADBF. Macrophage activation syndrome in the era of biologic therapy. Nat Rev Rheumatol. 2016; 12(259-268). |
| 10. | Schulert GS GA. Pathogenesis of macrophage activation syndrome and potential for cytokine-directed therapies. Annu Rev Med. 2015; 66(145-159). |
| 11. | 2000 EI. Neuroendocrine effects on immune system. In Endotext. (ed. De Groot LJ, et al.). MDText.com, South Dartmouth, MA. 2000. |
| 12. | Channappanavar R PS. Pathogenic human coronavirus infections: causes and consequences of cytokine storm and immunopathology. Semin Immunopathol. 2017 Julio; 39(529-539). |
| 13. | Huang C WYLXRLZJHYZLFGXJGXCZYTXJWYWWXXYWLHLMXYGHGLXJWGJRGZJQWJCB. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 Feb; 15(395). |
| 14. | Channappanavar R. Dysregulated Type I Interferon and Inflammatory Monocyte-Macrophage Responses Cause Lethal Pneumonia in SARS-CoV-Infected Mice. Cell Host Microbe. 2016 Febrero; 19(19181-193). |
| 15. | León A, Leija A, Garrido G, Reyes J, Rodriguez L. Tratamiento de la enfermedad. Rev Biomed. 2006; 17(195-211). |
| 16. | S. Martínez-Flórez JGGJMCyMJT. Los flavonoides: propiedades y acciones antioxidantes. Nutr. Hosp. 2002; XVII (6) 271-278. |
| 17. | Jassie S. LiveSciece. [Online].; 2015 [cited 2019 marzo 30. Available from: https://www.livescience.com/52524-flavonoids.html. |
| 18. | Coronado M, Vega y León S, Gutierrez R, Al igual que otros fitonutrientes, los flavonoides M, Radilla C. Antioxidants: present perspective. Rev Chil Nutr. 2015 Junio; 42(2). |
| 19. | Federico A DMLC. Silymarin/Silybin and Chronic Liver Disease: A Marriage of Many Years. Molecules. 2017 Jan; 22(2). |
| 20. | Michal B. Silybin, a Major Bioactive Component of Milk Thistle (Silybum marianum L. Gaernt.)—Chemistry, Bioavailability, and Metabolism. Molecules. 2017 Nov; 22(11):1942. |
x



Deja un comentario